Золото применяется во многих областях науки, техники, медицины, поскольку этот благородный металл не подвергается коррозии, а также обладает интересными электрическими, магнитными и оптическими свойствами.
1. Приведите конкретный пример использования золота в технике, а также пример использования золотых наночастиц в экспериментальных исследованиях. Кратко опишите суть исследования, и объясните, почему в нем оптимально использование именно золотых частиц нанометровых размеров. (2 балла)
Золото отличается высокой химической инертностью, проводимостью, и легко поддается обработке. Эти качества позволяют применять его, например, в электротехнике для создания контактов.
Ключевых моментов здесь два. Наночастицы золота все еще достаточно химически инертны, а их оптические и электрические свойства позволяют легко фиксировать их положение в различных системах. Поэтому в качестве типичного примера можно привести использование золотых наночастиц в качестве трейсеров, позволяющих оценивать микровязкость и проницаемость различных систем.
В этом вопросе максимальным баллом оценивается любой пример применения золота, который продемонстрирует возможность использования его, основываясь на его специфических свойствах.
Для многих применений золота необходимо, чтобы его поверхность была как можно менее дефектной. Механическая и даже электрохимическая полировка часто не позволяет достигнуть необходимой шероховатости поверхности. Недавно исследователи обнаружили неожиданное явление: растворение поверхности образца золота происходило под действием водного раствора перекиси водорода в присутствии сульфата железа (II) (реагент А).
2. Приведите два примера промышленного применения этого реагента, проиллюстрируйте их уравнениями реакций. (2 балла)
Реагент А (известный под названием «реагент Фентона») применяется в процессах, использующих гидроксил-радикалы, генерируемые по следующей реакции:
H2O2 = 2OH· (в этом случае железо выполняет исключительно каталитическую функцию). Предложен также иной механизм, включающий окисление железа: Fe2+ + H2O2 = Fe3+ + OH- + OH·.
Основными применениями считаются:
а) производство фенола из бензола (радикальное гидроксилирование аренов
б) Очистка сточных вод от хлорсодержащих органических соединений (оксиление органических соединений)
В качестве правильного ответа принимаются и другие примеры применения реагента Фентона – при указании источника на то, что описываемый процесс не является чисто лабораторным примером.
3. Под действием реагента А возможна полимеризация некоторых мономеров. Приведите уравнения химических реакций, протекающих на стадиях инициирования и роста цепи при полимеризации стирола в присутствии реагента А. Каким из способов (в блоке, в растворе, в эмульсии) возможна полимеризация а) метилметакрилата и б) акриламида при инициировании реагентом А? (2 балла) Зачем может быть необходимо введение наночастиц золота в полимеры (1 балл)?
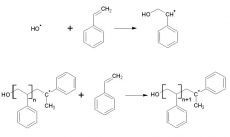
Инициирование и рост цепи происходят под действием генерируемых гидроксильных радикалов и описываются классической схемой (см. рис 2).
Так как реагент Фентона представляет собой водный раствор, полимеризация в блоке по определению невозможна с его участием. Акриламид – водорастворимый полимер, поэтому он может полимеризоваться как в растворе, так и в эмульсии типа «вода в масле». Метилметакрилат – гидрофобный, нерастворимый в воде мономер, поэтому единственная возможность инициировать его полимеризацию – система типа «масло в воде».
Возможен и синтез в обратной эмульсии – например, для метилметакрилата – типа «вода в масле». В этом случае инициатор находится в каплях водной фазы, инициирование процесса происходит на границе раздела фаз, а рост цепи – в органической фазе. Таким способом могут быть получены пористые образцы (генератор пор – капли водной фазы). Терминологически этот тип полимеризации может считаться полимеризацией в блоке, поэтому этот ответ принимается в качестве правильного при наличии обоснования.
По вопросу о введении золота в полимеры – принимаются абсолютно любые разумные реплики.
Известно, что металлическое золото хорошо растворяется в концентрированном растворе неорганических цианидов в присутствии воздуха.
4. Запишите уравнения протекающих при этом реакций. Объясните, почему присутствие цианид-иона способствует растворению золота. (1 балл)
4Au + 8CN- + O2 + 2H2O= 4[Au(CN)2]- + 4OH-
Присутствие цианид-ионов связывает золото в прочный комплекс, таким образом сдвигая равновесие реакции вправо.
Принимается и объяснение, основанное на выражении для условного потенциала Нернста в присутствии комплексообразователей.
Под действием реагента А происходит растворение дефектов поверхности золота, а гладкая поверхность инертна к действию этого реагента. Этот результат крайне важен, потому что позволяет получить практически бездефектную поверхность, например, для использования в медицинских имплантантах. Известно, что иммунный ответ на введение имплантантов по механизму действия аналогичен реагенту А, поэтому такая обработка позволит избежать выделения золота (тяжелого металла) в организме.
Было продемонстрировано, что под действием реагента А происходит выравнивание предварительно механически отполированной поверхности, при этом реальная площадь поверхности уменьшается на 40%. На рис. 1 приведено изображение исходной поверхности золота.
5. Оцените, сколько золота выделяется с поверхности имплантанта площадью 100 см2 (для расчетов примите, что дефекты можно представить полусферами. Необходимые геометрические параметры приближенно определите из рис. 1). Приняв, что за время реакции выделившееся золото диффундирует в объем 5 л, предложите аналитические методы определения таких количеств золота. (4 балла)
Начнем с того, что, по всей видимости, решить эту задачу в общем виде невозможно, поэтому ответ будет зависеть от вводимых упрощений. Оценивается любое разумное решение при наличии обоснования и корректных расчетов.
Предположим, что поверхность золота после обработки реагентом Фентона идеально гладкая, а имеющиеся на исходной поверхности дефекты – правильные полусферы с радиусом 1 мкм (10-6 м). Тогда каждая такая полусфера увеличивает реальную площадь поверхности на (2pR2 – pR2 = pR2) – разность между площадью поверхности полусферы и ее проекции на плоскость – круга равного радиуса. Если исходная площадь поверхности S=100см2 = 10-2м2, то площадь поверхности после удаления N полусферических дефектов равна S'=S-NpR2 = 10-2 – NpR2 = 6·10-3м2, откуда N ~ 109. Суммарный объем этих полусфер равен 109·0.5·4/3pR3 ≈ 2·10-9 м3. Масса этого объема золота равна 0.04 г, а значит, его концентрация в тканях 0.008 г/л.
Несмотря на то, что масса золота достаточно велика, нужно принимать во внимание характер анализируемого объекта. У живого человека затруднительно отобрать для анализа 5 л образца. Пусть объем пробы составит 100 мл, тогда масса золота в нем 0.0008 г. Для обнаружения 0.8 мг золота неприменимы гравиметрические методы с пределом обнаружения от 1-2 мг (за исключением специальных методов, например, с использованием меркаптобензотиалола – оценивается при наличии указания на подходящую весовую форму). Типичные титриметрические методы не позволяют достичь требуемого результата (предел обнаружения от 2-5 мг), но, например, титрование гидрохиноном с подходящим индикатором решает требуемую задачу. Один из подходящих методов определения микроколичеств золота – фотометрия наночастиц, образующихся в контролируемых условиях. Принимаются и другие подходящие способы, перечислить которые все не позволяет время.