Все соединения и известные объекты состоят из атомов – стулья, столы, продукты, вода, грифель карандаша (да и сам карандаш). В том числе и наноструктуры. Поэтому, прежде чем вводить понятия различных наноструктур (фуллеренов, нанотрубок и т. д.) необходимо разобраться с тем, что же такое атом.
Атом
Так что же такое атом? Известна простейшая модель для его описания, которая была придумана почти 100 лет назад – Модель Резерфорда
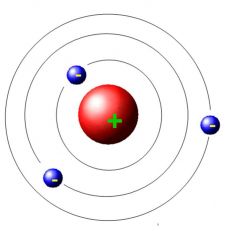
Представать её себе можно так: есть большое положительно заряженное ядро – такой большой красный шарик с зарядом “+”. Вокруг этого красного шарика, как планеты вокруг Солнца, летают электроны – маленькие синие шарики с зарядом “–“ (см. рис. 1а).
Имеется одна особенность, связанная с величиной заряда синих шариков – электронов. Во-первых, заряды всех электронов равны, а, во-вторых, сумма зарядов всех электронов, летающих вокруг красного шарика – ядра, равна по модулю заряду ядра.
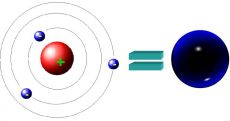
Это и есть модель Резерфорда. Её ещё иногда называют планетарной, поскольку ядро в такой модели атома играет роль Солнца, а электроны – планет, вращающихся вокруг Солнца как в нашей Солнечной Системе. Таким образом, такая структура: из красного шара внутри и синих вокруг него, и есть атом – в дальнейшем большой шар (см. рис. 1б.)
Связь между атомами. Молекула.
Все молекулы состоят из атомов, причём, связанных между собой атомов. Простейшие молекулы представляют собой два связанных атома. Например, молекула водорода, в которой связываются два атома водорода. Есть и сложные молекулы - например, молекулы полимеров, в которых между собой связывается очень большое число атомов.
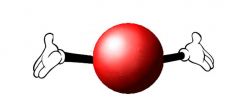
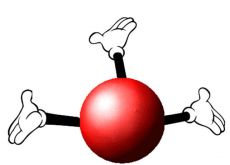
О том, что же такое атом нам известно. Что же такое связанные атомы? Разобраться с этим можно очень просто на таком примере. Представьте, что Вы – атом. Не вдаваясь в структуру атома, просто Вы сейчас – атом. Вместо большого шарика, описанного выше, будете Вы. Пусть у Вас есть друг. И он тоже – атом. Тогда, если Вы с другом находитесь достаточно близко, то можете держаться за руки (см. рис. 2а). А когда расстояние между Вами очень велико (например, несколько километров), то взяться за руки довольно сложно (если у Вас, конечно, не километровые руки). Однако будем считать, что Ваши руки нормальной длины (см. рис. 2б).
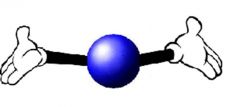
Таким образом, когда Вы близко друг к другу и можете держаться за руки, будем говорить, что Вы (атомы) – связаны. В том же случае, когда Вы отошли друг от друга на значительное расстояние и уже не можете держаться за руки - Вы не связаны. Также и реальные атомы: могут быть связаны, когда они рядом, и не связаны, когда они далеко. (см. рис. 3а, б.)
При этом атомы связываются за счёт своих свободных {Прим.: "валентных"} электронов: сколько есть у атома свободных электронов, столько и связей он может создать. В связанных атомах электроны могут прыгать от одного атома к другому.
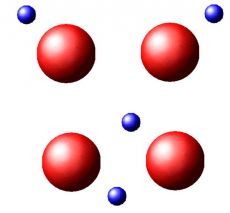
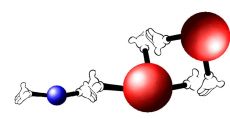
Наглядно на шариках это выглядит так: синий шарик сначала был расположен около одного атома, а потом прыгнул на другой и стал большую часть времени сидеть около него – см. рис. 4.
Если атом – это человек, то число возможных связей – это число рук у него (оно равно числу свободных электронов). Рис.5
Пусть у Васи две руки, а у Миши их три – см. рис. 6а, б.
Тогда Вася, взявшись своими двумя руками за две Мишины руки, образует с ним две связи, а, значит, молекулу Вась-Миша. Однако у Миши всё ещё одна рука свободна, ей он может ещё кого-нибудь схватить за свободную руку и присоединить к молекуле Вась-Миша, например, Катю. Тогда будет молекула из трёх атомов – Вась-Миш-Катя. Рис.7
У ребёнка, играющего роль атома углерода, всего 12 рук (электронов). Из них 8 рук (электронов) плотно привязаны к телу (поскольку у атома углерода только 4 внешних электрона, способных образовывать связь). Этими прижатыми руками невозможно даже пошевелить. Оставшиеся четыре руки – не связаны. Ими он может брать за руки других детей и образовывать связанные углеродные молекулы и кластеры – скопления атомов углерода (детей, держащихся друг за друга).
В чём же реальность примера? Например, из атомов углерода (обозначаются они как “С”) состоит, грифель карандаша.







 Для физиков и "валентных" электронов нет. Для химика радикалы имеют "неспаренные" электроны. Везде условности, но суть автор выразил верно, несправедливо его обвинять в неиспользовании терминологии, то есть того, чего он и не собирался использовать изначально.
Для физиков и "валентных" электронов нет. Для химика радикалы имеют "неспаренные" электроны. Везде условности, но суть автор выразил верно, несправедливо его обвинять в неиспользовании терминологии, то есть того, чего он и не собирался использовать изначально.
