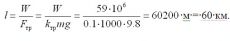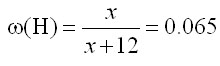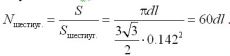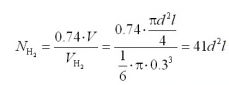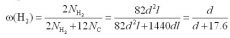Нанотрубки для водородной энергетики
Решение
1. Водород: H2 + ½ O2 = H2O(ж) DH = 286 кДж/моль H2 = 143 кДж/г H2
Углерод: C + O2 = CO2 DH = 393 кДж/моль С = 33 кДж/г C
Метан:СH4 + 2O2 = CO2 + 2H2O(ж) DH = 890 кДж/моль CH4 = 56 кДж/г CH4
Бензин: C8H18 + 25/2 O2 = 8CO2 + 9H2O(ж) DH = 5616 кДж/мольC8H18 = 49 кДж/гC8H18
Водород имеет наибольшую удельную теплоту сгорания.
2. Для реакции
H2 + ½ O2 = H2O(ж), которая протекает в водородном топливном элементе, изменение энергии Гиббса при 298 К равно:
DG = DH – TDS = –286 – 298×(–163×10–3) = –237 кДж/моль H2 = – 119 кДж/г H2.
Работа, совершенная при сгорании
Расстояние равно работе, деленной на силу трения (Формула 1): 60 км.
3. Наибольшая массовая доля водорода – в метане, CH4. Она составляет 25%. Водород (100% водорода) - простое вещество!
4. Каждый атом углерода в графите или нанотрубке может присоединить один атом водорода. В этом случае массовая доля водорода максимальна и равна 1 / (1+12) = 0.077 = 7.7%.
Пусть 1 моль С присоединил x моль H, тогда массовая доля водорода составит (Формула 2) x = 0.83. Доля связанных атомов углерода составит 83%, то есть примерно 5/6.
5. Нанотрубка имеет форму цилиндра длиной l и диаметром d. Объем трубки V = pd2l / 4, ее поверхность S = pdl. Число шестиугольников на поверхности трубки равно отношению площади трубки к площади шестиугольника (Формула 3). Каждый атом углерода принадлежит трем шестиугольникам, следовательно на один шестиугольник приходится 6/3 = 2 атома углерода, значит общее число атомов C в нанотрубке: NC = 120dl.
Найдем число молекул водорода. Известно, что шары при плотнейшей упаковке занимают 74% от объема пространства. Число шаров в полости трубки равно отношению 74% объема трубки к объему молекулы (Формула 4). Массовая доля водорода (Формула 5), где d выражено в нм. При диаметре 3 нм массовая доля водорода внутри трубки может достигать 15%.
Автор – проф. В.В.Еремин