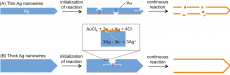
Иногда требуется получить наноструктуры, полые изнутри. И если углеродные нанотрубки сами собой растут полыми, то для получения полых металлических наноструктур: нанотрубок или “клеток” (то есть оболочек кубика) - приходится повозиться. К счастью, уже существует технология так называемого гальванического замещения, делающая это возможным. Идея ее проста и понятна: изготовляется шаблонная сплошная наноструктура из более активного металла и помещается в раствор менее активного металла. После этого активный металл постепенно окисляется и растворяется, а на его поверхности растет слой менее активного металла, восстанавливающегося из раствора. И так происходит, пока более активный металл внутри наноструктуры не растворится полностью.
Группа американских ученых выращивает таким способом полые нанотрубки золота с использованием сплошных нанонитей серебра. В качестве прекурсора золота они используют раствор HAuCl4, постепенно окисляющий серебро, согласно уравнению:
3Ag + AuCl4- --> 3Ag+ + 4Cl- + Au
Казалось бы, ион серебра с ионом хлора должны образовывать твердые частицы хлорида серебра, но этого не происходит, так как концентрация ионов серебра мала и произведение растворимости AgCl не превышается.
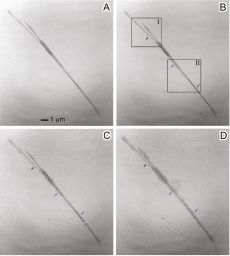
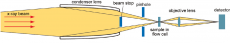
Для изучения механизма протекания процесса исследователи следили за ним in situ при помощи просвечивающего рентгеновского (!) микроскопа. (Применение просвечивающего электронного микроскопа в данном случае невозможно из-за чрезмерного поглощения электронов раствором, а тонкий слой раствора не позволит свободно протекать гальваническому замещению).
Удалось обнаружить, что растворение серебра начинается в районе дефектов нанонити, видимых в качестве ямок на ее поверхности. Это связано с тем, что там кристаллическая решетка искажена и атомы обладают дополнительной энергией. Тонкие нанонити при этом могут фрагментироваться, что приводит к получению отдельных кусков нанотрубок. В случае более толстых нанонитей, получается сплошная протяженная нанотрубка, а дефект на этом месте впоследствии (после полного растворения серебра) заращивается.