Нанотехнология – область научного знания, направленная на решение технологических проблем, связанных с манипуляцией материей (атомами и молекулами) в диапазоне от 1 до 100 нанометров (10-9 м). При уменьшении размера изучаемого объекта до масштабов 100 и менее нм на смену классическим физическим законам взаимодействия между атомами и молекулами приходят квантовые, например, туннельные переходы и поверхностный плазмонный резонанс (ППР). Система, имеющая размеры нанометрового диапазона, может быть описана с позиции термодинамики нелинейных процессов [1]. Таким образом, используя нанотехнологический подход в решении некоторых медицинских проблем, можно качественным образом изменить медицинскую науку.
Выделяют несколько направлений, где нанотехнологии успешно применяются: 1. Доставка лекарственных средств (молекул) до мишени; 2. Лечение и протезирование с использованием наноматериалов; 3. Диагностика.
Доставка лекарств
Несмотря на широкий арсенал лекарств, применяемых в медицине, одной из важнейших проблем остается их адресная доставка с целью повышения эффективности лечения [2]. Обычно, лекарственная субстанция после адсорбции распределяется по тканям организма относительно равномерно. В частности противоопухолевые препараты не только подавляют деление трансформированных клеток, но и активно делящихся нетрансформированных клеток. С этим связаны побочные эффекты многих цитостатиков [3]. Сильные побочные эффекты противоопухолевых лекарственных средств делают терапию малоэффективной. При этом качество жизни пациента не только не улучшается, но в некоторых случаях снижается [4].
С внедрением новых подходов для решения проблемы адресной доставки лекарств позволит значительно улучшить не только качество жизни пациентов за счет снижения побочных эффектов, но повысить избирательность, следовательно, и эффективность лечения. Используют различные способы загрузки лекарственных молекул для адресной доставки, например, капсулирование и конъюгирование. Адресная доставка лекарств при противоопухолевой терапии позволит разрешить несколько проблем [5]:
- Защитить лекарства от деградации и нежелательных взаимодействий с биологическими молекулами;
- Увеличить селективную абсорбцию лекарств опухолевыми клетками;
- Контроль за фармакокинетикой;
- Увеличить биодоступность лекарств внутрь опухолевых клеток.
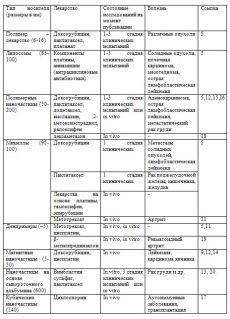
Многие трансформированные (раковые) клетки имеют на своей поверхности либо специфические рецепторы, либо усиленно продуцируют рецепторы, характерные для нетрансформированного состояния [5-8]. Например, CD19 экспрессируется на всех неопластических клетках острых лейкозов В-клеточного происхождения, а также присутствует при некоторых формах острых монобластных лейкозов. Число копий на поверхности может достигать 104-105на 1 клетку. Эти свойства можно использовать для доставки лекарств к опухолевым клеткам, предварительно конъюгируя антитела к этим рецепторам с наночастицами. Таким образом, за счет антитело-антигенного взаимодействия достигается адресная доставка противоопухолевого лекарства до трансформированных клеток [5]. Аналогичен подход при терапии рака простаты. Одним из важных маркеров рака простаты, иногда некоторых карцином является простатический специфический мембранный антиген (PSMA). Конъюгат антител к PSMAс дендримерами можно использовать для доставки лекарств непосредственно к поверхности клеток рака простаты [7]. На сегодняшний день предполагается более 200 систем (платформ) адресной доставки противоопухолевых и других лекарств, в том числе основанных на антителах или их фрагментах, часть из них проходит доклинические и клинические испытания. Некоторые из них представлены в таблице 1 [9-21]. Помимо лекарственных средств с помощью наночастиц возможно доставлять внутрь клетки гены [22].
Наноматериалы в качестве лекарственных средств
Наноматериалы возможно использовать не только как средство доставки лекарственных молекул к мишеням, их можно непосредственно использовать как лекарства. Это обеспечивается уникальными магнитными и оптическими свойствами наноматериалов [1].
Многие линии раковых клеток, в отличие от нетрансформированных, чувствительны к температуре 40оС и выше [23,24]. Магнитные наночастицы из Fe3O4 можно нагреть, если их поместить в переменное магнитное поле [25]. Модифицируя поверхность магнитных наночастиц, например, лютеинизирующим гормоном, рецепторы которого усиленно экспонированы на клетках рака молочной железы, можно получить терапевтическое средство, которое при помещении в магнитное поле будет нагреваться, поражая трансформированные клетки [26].
Наравне с гипертермией используется фотодинамическая терапия рака, которая заключается во введении фотосенсебилизатора в опухоль и облучении ее светом определенной дины волны, как правило, инфракрасным (ИК). При этом генерируются активные формы кислорода, убивающие раковые клетки [27]. Однако ИК излучение, во-первых, несет мало энергии, во-вторых, не может глубоко проникать, особенно в крупные опухоли. В настоящее время есть попытки в качестве глубоко проникающего излучения использовать рентгеновское [28].
Радиотерапия – традиционный способ лечения рака, в сочетании с химиотерапией он дает неплохие результаты, однако побочные эффекты иногда настолько сильны, что данный подход иногда не применим вовсе. Одной из причин малой эффективности радиотерапии является неизбирательность изучения при воздействии на организм. При облучении наравне с опухолевыми клетками повреждаются и здоровые [29]. Для увеличения селективности радиотерапии используют модифицированные наночастицы золота или других металлов. Такие наночастицы вводя либо в кровоток, либо местно, затем опухоль облучают γ-лучами [30].
Водорастворимый фуллерен (С60) был предложен для лечения артритов. Ревматоидный артрит – хроническое воспалительное заболевание характеризующийся синовиальной гиперплазией с неоангиогенезом и инфильтрацией лимфоцитов и макрофагов в синовиальную ткань. С60 – сферические углеродные наномолекулы, обладающие антиоксидантными свойствами, защищающие от дегенерации суставной хрящ катаболически индуцированного остеоартрита, также являются активаторами хондрогенеза [31].
Уникальные свойства наноматериалов позволяют изготавливать различные имплантаты и протезы. С использованием нанотехнологий можно получить безопасные, биосовместимые и прочные имплантаты. Хорошо зарекомендовали себя наноматериалы на основе полимеров и металлополимерных нанокопозитов [32] и гидроколлоидов жидкокристаллической гидроксипропилцеллюлозы и слоистых алюмосиликатов [33]. Гидроколлоидные композиции – многокомпонентные полимерные системы, содержащие как гидрофобную, так и гидрофильную фазы, находят широкое применение на рынке медицинских и косметических препаратов для лечения различных нарушений кожных покровов и поверхностных мышечных тканей и их предотвращения. Несколько крупных фирм (Johnson&Johnson,Schering-Plough, Coloplast, Procter&Gamble, 3M, Smith&Nephewи др.) работают в области улучшения таких свойств гидроколлоидов, как адгезия, способность сорбировать большое количество биологических жидкостей, выделяющихся из поврежденных участков, отсутствие травмирования здоровых участков кожи при снятии пластыря-покрытия, поглощение неприятного запаха, смягчающий эффект, прозрачность, дающая возможность визуализировать процесс заживления без снятия повязки в течение нескольких суток и др. Нанотрубки из оксида титана обладают остеоинтегративным эффектом [34]. Сочетание полиметилметакрилата с наночастицами циркония и сульфата бария дает возможность улучшить качество костных имплантатов [35].
Биосенсоры
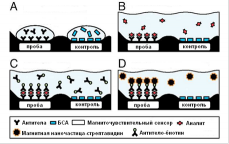
Развитие нанотехнологий в биомедицине связано с усовершенствованием технологий и методов визуализации, характеристики и анализа биоматериала, обеспечивающие высокую степень разрешения порядка менее 10-6м [36]. Магнитные наноматериалы являются важным источником для получения биосенсоров. Чаще всего используют наночастицы на основе оксида железа покрытые оболочкой из различных полимеров. Поверхность модифицируют различными биоспецифическими лигандами. При этом оболочка защищает наночастицы оксида железа от химического взаимодействия с молекулами клеток и тканей. Существует два способа связывания биосенсоров с детектируемой поверхностью: 1. Прямой способ и 2. Косвенный, по типу сэндвича см. рисунки 1 и 2 [37].
В первом случае функционализированные магнитные наночастицы специфическими антителами непосредственно взаимодействуют с антигенами. Этот способ обладает относительно малой чувствительностью, а образовавшиеся конъюгаты агрегируют и выпадают в осадок. Во втором случае, чувствительность достигается опосредованным взаимодействием стрептавидина с биотином.
Гадолиний, особенно в сочетании с кобальтом или железом обладает уникальными магнитными свойствами. Атомы гадолиния, обладая парамагнитными свойствами, генерируют локальное магнитное поле, которое ускоряет переориентацию протонов окружающих молекул воды, индуцируемого магнитным полем магнитно-резонансного томографа (МРТ). Хелатирование Gd(III) с различными комплекообразователями с последующее конъюгацией с функционализированными наночастицами позволяет получить комплекс Gd-(хелат)-дендример-фолиевая кислота, который способен связываться с фоллат-специфическими рецепторами раковых клеток. Таким образом, возможна визуализация опухолей с высокой разрешительной способностью и особенно для выявления метастаз [38].
Помимо оптических свойств в биодетекции используют оптические и электрохимические свойства наноматериалов. Так, для фуллеренола в комплексе с ДНК наблюдается усиление флюоресценции. Минимальная концентрация ДНК, определяемая флюоресцентным методом, составляет 1,3 пг на 1 мл [39].
Идея использования наночастиц золота (НЧЗ) в качестве меток нуклеотид-нуклеотидных взаимодействий не нова. Частицы НЧЗ в комплексе с поли(dТ) последовательностями использовались еще в 1981 г. для картирования политенных хромосом методом гибридизации in situ на электронно-микроскопическом уровне. Новый импульс в использовании НЧЗ в качестве меток биоспецифических маркеров был придан введением в практику пришивки макромолекул посредством тиольных производных. Такие маркеры существенным образом отличаются от традиционно используемых в электронной цито- и гистохимии, основанных на исключительно адсорбционных, ван-дер-ваальсовых и гидрофобных взаимодействиях метки (НЧЗ) и зонда (биомолекулы). Тиольные производны НЧЗ с биомелекулами обеспечиваются связью с энергией 40 ккал/моль (RS-H). При взаимодействии функционализированных НЧЗ с молекулами мишенями происходит изменение оптических свойств системы. Чувствительность может достигать 3 нг/мл [40]. Помимо НЧЗ используют наночастицы наночастицы серебра, кобальта, платины и т.д. [41].
В качестве электрохимических сенсоров используют функционализированные квантовые точки [42], нанотрубки и наночастицы [43]. Таким образом, используя уникальные свойств наноматериалов в качестве биосенсоров, позволит повысить на качественно высокий уровень современную медицинскую диагностику таких социально значимых заболеваний как рак, инфекционные и нейро-дегенеративные.
Отдельно следует отметить биочипы, которые были изобретены в конце 90-х годов одновременно в России и США. Широкое распространение получили ДНКовые и белковые биочипы. Сегодня биочипы находят в процессе своего развития в качестве аналитических устройств, позволяющие получать и перерабатывать экспресс-информацию о химическом составе изучаемый объектов [36].
Заключение
В представленном мини-обзоре по использованию нанотехнологий в медицине представлена лишь малая часть результатов исследований проводимых в самых различных научных лабораториях и центра мира. Число научных журналов, публикующих работы по наномедицине исчисляется сотнями и с каждым годом увеличивается. Таким образом, происходит накопление экспериментальных данных, осуществляется разработка новых технологий для нужд медицины. Широкое внедрение в медицинскую практику ждут с нетерпением миллионных больных в разных уголках земного шара. На мой взгляд, использование классических методов лечения в сочетании с нанотехнологиями позволит напорядок улучшить качество терапии сердечнососудистых и инфекционных заболеваний, рака.
Литература
- Суздалев И.П. Нанотехнология: физикохимия нанокластеров, наноструктур и наноматериалов. М.: КомКнига, 2006. 592с.
- A German initiative on health aspects of synthetic nanoparticles: creation of an information and knowledge information-base for innovative material research knowledge. Bundesministerium fur bildung und forschung. 2008.
- Маркман М., Уалкер Дж.Л. Внутрибрюшинная химиотерапия при раке яичников: обзор литературы, практические рекомендации по лечению // Клиническая онкология 2006. Т.24. № 6. С.50-56
- Гурина Л.И. Побочные эффекты гормонотерапии рака предстательной железы // Росс. онкол. журнал. 2003. № 3. С. 15–19.
- Perr D., Karp J.M., Hong S., Farokhzad O.C., Magalit R., Langer R. Nanocarriers as an emerging platform for cancer therapy // Nature nanotechnology 2007. V.2. №12. P.751-760
- Brannon-Peppas L., Blanchette J.O. Nanoparticle and target systems for cancer therapy // Advanced drug delivery reviews 2004. V.56. P.1649-1659
- Parti A.K., Myc A., Beals J. et al Synthesis and in vitro testing of J591 antibody – dendrimer conjugates from target prostate cancer therapy // Bioconjugate chem. 2004. V.15. P.1174-1181
- Shukla R., Thomas T.P., Peters J.L. et al. Her2 specific tumor targeting with dendrimer conjugate anti-her2 mAb // Bioconjugate chem. 2006. V.10. P.1385-1399
- Chen B., Lai B., Cheng J. et al. Daunorubicin-loaded magnetic nanoparticles of Fe3O4 overcome multidrug resistance and induce apoptosis of K562-n/VCR cell in vitro // Inter. J. of Nanomedicine 2009. V.4. P.201-208
- Jing Z., Chen B., Xia G-H. et al. The reversal effect of magnetic Fe3O4 nanoparticles loaded with cisplatin on SKOV3/DDP ovarian carcinoma cells // Inter. J. of Nanomedicine 2009. V.4. P.107-114
- Haririan I., Alavidjeh M.S., Khorramizadeh M.R. et al. Anionic linear-globular dendrimer-cis-platinum (II) conjugates promote cytotoxicity in vitro against different cancer cell lines // Inter. J. of Nanomedicine 2010. V.5. P.63-75
- Martis D., Frugillo L., Anazzetti M.C., et al. Antitumoral activity of L-ascorbic-poly-D,L-(lactide-co-glycolide) nanoparticles containing violacein // Inter. J. of Nanomedicine 2010. V.5. P.77-85
- Zu Y., Zhang Y., Zhao X. et al. Optimization of the preparation process of vinblastine sulfate (VBLS)-loaded folate-conjugated bovine serum albumin (BSA) nanoparticles for tumor-targeted drug delivery using response surface methodology (RSM) // Inter. J. of Nanomedicine 2009. V.4. P.321-333
- Yu M.K., Jeong Y.Y., Park J. et al. Drug-loaded superparamagnetic iron oxide nanoparticles for combined cancer imaging and therapy in vivo // Angew. Chem. Int. Ed. 2008. V.47. P.5362-5365
- Shi X., Wang S., Chen X. et al Encapsulation of submicrometer-sized 2-methoxyestradiol crystals into polymer multilayer capsules for biological applications // Molecular pharmaceutics 2006. V.3. №2. P.144-151
- Bikiaris D., Karavelidis V., Karavas E. Novel biodegradable polyesters. Synthesis and application as drug carriers for the preparation of raloxifene Hcl loaded nanoparticles // Molecules 2009. V.14. P.2410-2430
- Lai J., Lu Y., Yin Z. Hu F., Wu W. Pharmacokinetics and enhanced oral bioavailability in beagle dogs of cyclosporine A encapsulated in glyceryl monooleate/poloxamer 407 cubic nanoparticles // Inter. J. of Nanomedicine 2010. V.5. P.13-23
- Zhang L., Li Y., Zhang Ch., Wang Y., Song C. Pharmacokinetics and tolerance study of intravitreal injection of dexamethasone-loaded nanoparticles in rabbits // Inter. J. of Nanomedicine 2009. V.4. P.175-183
- Hwang J., Rodgers K., Oliver J.C., Schluep Th. α-Methylprednisolone conjugated cyclodextrin polymer-based nanoparticles for rheumatoid arthritis therapy // Inter. J. of Nanomedicine 2008. V.3. P.359-371
- Miele E., Spinelli G.P., Miele E., Tomao F., Tomao S. Albumin-bound formulation of paclitaxel (Abraxane ABI-007) in the treatment of breast cancer // Inter. J. of Nanomedicine 2009. V.4. P.99-105
- Зыкова М.Г., Прозоровский В.Н., Ипатова О.М., Торховская Т.И., Глазатов В.В. Антиревматоидная активность метотрексата, включенного в фосфолипидные наночастицы (фосфоглив) // Биомедицинская химия 2007. Т. 53. № 4. С.435-441
- McMain S.C., Yiu H.HP., Dobson J. magnetic nanoparticles for gene and drug delivery // Inter. J. of Nanomedicine 2008. V.3. P.169-180
- Luk K.H., Hulse R.M., Phillips T.L. Hyperthermia in cancer therapy // The Western J. of Medecine 1980. V.132. P.179-185
- Зинченко В.А. О мехнизмах комбинировнаного действия гипертермии и радиации на опухолевые клетки // Биополимеры и клетка 1998. Т.14. № 2. С.93-98
- Goya G.F., Grazu V., Ibarra M.R. Magnetic nanoparticles for cancer therapy // Current Nanoscience 2008. V.4. P.1-16
- Jin H., Hong B., Kakar Sh.S., Kang K.A. Tumor-specific nano-entities for optical detection and hyperthermic treatment of breast cancer // Advances in experimental medicine and biology 2008. V.614. P.275-284
- Praetorius N.P., Mandal T.K. Engineered nanoparticles in cancer therapy // Recent patents on drug delivery and formulation 2007. V.1. P.37-51
- LiuY., Chen W., Wang S., Joly A.G. Investigation of water-soluble x-ray luminescence nanoparticles for photodynamic activation // Appl. Phys. Lett. 2008. V.92. № 4. P. 2835701-2835707
- Juzenas P., Chen W., Sun Y-P. et al. Quantum dots and nanoparticles for photodynamic and radiation therapies of cancer // Adv. Drug Deliv. Rev. 2008 . V.60. № 15. P.1600–1614
- Zhang X-D., Guo M-L., Wu H-Y. Irradiation stability and cytotoxicity of gold nanoparticles for radiotherapy // Inter. J. of Nanomedicine 2009. V.4. P.165-173
- Yudoh K., Karasawa R., Masuko K., Kato T. water-soluble fullerene (C60) inhibits the development of artrits in the rat model of arthritis // Inter. J. of Nanomedicine 2009. V.4. P.217-225
- Помогайло А.Д. Металлополимерные нанокомпозиты с контролируемой молекулярной архитектурой // Рос. хим. ж. (Ж. Рос. Хим. Об-ва им. Д.И. Меделеева) 2002. Т. XLVI. № 5. С.64-73
- Куличихин В.Г., Антонов С.В., Макарова В.В., Семаков А.В., Singh P. Нанокомпозитные гидроколлоидные адгезивы для биомедицинского применения // Российские нанотехнологии 2006. Т.1. №1-2. С.170-182
- Slu Y-T. Electrochemical growth behavior, surface properties and enhanced in vivo bone response of TiO2 nanotubes on microstructured surfaces of blasted, screw-shaped titanium implants // Inter. J. of Nanomedicine 2010. V.5. P.87-100
- Gillani R., Ercan B., Qiao A., Webster Th. Nanofunctionalized zirconia and barium sulfate particles as bone cement additives // Inter. J. of Nanomedicine 2010. V.5. P.1-11
- Сарвилина И.В., Каркищенко В.Н., Горшкова Ю.В. Междисциплинарные исследования в медицине. М.: Техносфера, 2007. 368с.
- Koh I., Josephson L. Magnetic Nanoparticle // Sensors 2009. V.9. P.8130-8145
- Swanson S.D., Kukowska-Latallo J.F., Patri A.K. et al. Targeted gadolinium-loaded dendrimer nanoparticles for tumor-specific magnetic resonance contras enhancement // Inter. J. of Nanomedicine 2008. V.3. P.1-10
- Pinteala M., Dascalu A., Ungurenasu C. Binding fullerenol C60(OH)24 to dsDNA // Inter. J. of Nanomedicine 2009. V.4. P.193-199
- Дыкман Л.А., Богатырев В.А., Щеглов С.Ю., Хлебцов Н.Г. Золотые наночастицы: синтез, свойства, биомедицинское применение. М.: Наука, 2008. 319с
- Ершов Б.Г. Наночастицы металлов в водных растворах: электронные, оптические и каталитические свойства // Рос. хим. ж. (Ж. Рос. хим. об-ва им. Д.И. Менделеева) 2001. Т. XLV. № 3. С. 20-30
- Drbohlavova J., Adam V., Kizek R., Hubalek J. Quantum dots – characterization, preparation and usage in biological systems // In. J. Miol. Sci. 2009. V.10. P.656-673
- Qi H., Peng Y., Gao Q., Zhang Ch. Application of nanomaterials in electrogenerated chemiluminescence biosensors // Sensors 2009. V.9. P.674-695