В последнее время, благодаря быстрому развитию нанотехнологий, был достигнут значительный прогресс в этой области. Например, присоединяя к квантовым точкам антитела, можно получить синтетические нанообъекты для наблюдения за клетками [3]. Но несмотря на успех в создании наноструктур и пришиванию их ковалентными связями к клеточной поверхности, у биологов и медиков остается задача, как заставить синтетические нанообъекты взаимодействовать с клеточной машиной [4].
Есть несколько путей, которыми наноматериал попадает в клетку. Основная проблема в каждом из них - это необходимость преодолеть клеточную мембрану, поэтому необходимо создавать небольшие молекулы, которые легко смогут пройти через нее, и строить из них наноструктуру внутри клетки. Однако большинство процессов, которые можно использовать для образования таких ковалетных связей, протекают в неводной и даже в нефизиологической среде, что несовместимо с клеточной средой. Таким образом, можно выделить следующие требования к подобным реакциям:
- биосовместимость - необходимо свести к минимуму число реакций с компонентами клетки,
- эффективность - реакция должна протекать с разумной скоростью даже при низкой концентрации реагента,
- локальность - реакция должна протекать только внутри клетки или даже только в одном специфическом месте клетки, и, наконец,
- возможность точного контролья - реакция должна протекать только тогда, когда требуется.
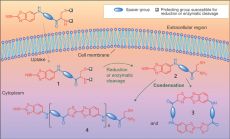
Лучше всего такие реакции проводит Природа. Например, светлячки производят люциферин - небольшие молекулы, отвечающие за их желто-зеленое свечение, - в ходе конденсации 2-цианобензотиазола (ЦБТ) с 1,2-аминтиолом в D-цистеине [5]. Вдохновленные этим, ученые создали ряд прекурсоров, например, как 1 на Рис. 1, в которых ЦБТ присоединен к защищенной 1,2-аминтиольно группе небольшим спейсером (например, одиночная молекула амина). Прекурсор 1 имеет небольшой молекулярный вес, растворим в воде и может преодолеть клеточную мембрану. Защитная группа создана так, что через час после попадания в клеточную мембрану она удаляется либо в ходе восстановления, либо в ходе гидролиза. В результате образуется свободный 1,2-аминотиол (2), который затем претерпевает самоконденсацию с образованием димера (3) и олигомеров (4), которые, в свою очередь, могут собираться в наноструктуры. Кроме довольно высокой константы скорости [6], что редкость для биосовместимых реакций, одной из заметных особенностей этой реакции является то, что она контролируется молекулами, уже существующими внутри клетки в ходе специфического восстановления и/или ферментативного расщепления.
Изучая различные мономеры, ученые показали, что конденсация контролируемо протекает в водной среде. Форму, размер и собственно собирающуюся наноструктуру можно контролировать, изменяя структуру исходного мономера. На следующем этапе они получили мономер, снятие защиты в котором происходит внутри клетки, и успешно провели внутриклеточную реакцию конденсации. Присоединенный к прекурсорам биотиновый хвостик позволил отслеживать образование продукта с помощью флуоресценции. Когда под действием фермента фуринпротеазы отщеплялись защитные группы, продукт собирался около зоны Гольджи, где и располагается белок фурин. По изменению флуоресцентных свойств можно судить и о дальнейшей конденсации агрегата с образованием нерастворимых осадков. Это особенно ценно, поскольку специальный фермент может отследить расположение синтетической наноструктуры внутри клетки. Это может иметь множество практических применений, например, как уже было показано, для визуализации злокачественных опухолей и направленного переноса лекарственных средств. А именно, присоединяя лекарство от рака или визуализирующий материал, можно провести селективную конденсацию в опухолевых клетках.
Использование небольших молекул для строительства наноструктур внутри клеток может стать новым способом понимания и регулирования происходящих в клетках превращений, что раньше было затруднено из-за небольшого числа биосовместимых реакций.